藥物臨床試驗機構備案要求及常見問題分析
2019-12-01藥物臨床試驗機構(簡稱機構)開始實行備案管理。本文結合機構備案平臺構建思路,著重介紹了備案平臺的結構組成以及相關要求,梳理了機構備案過程中的常見問題,對機構
來源:醫療器械注冊代辦 發布日期:2024-11-07 閱讀量:次
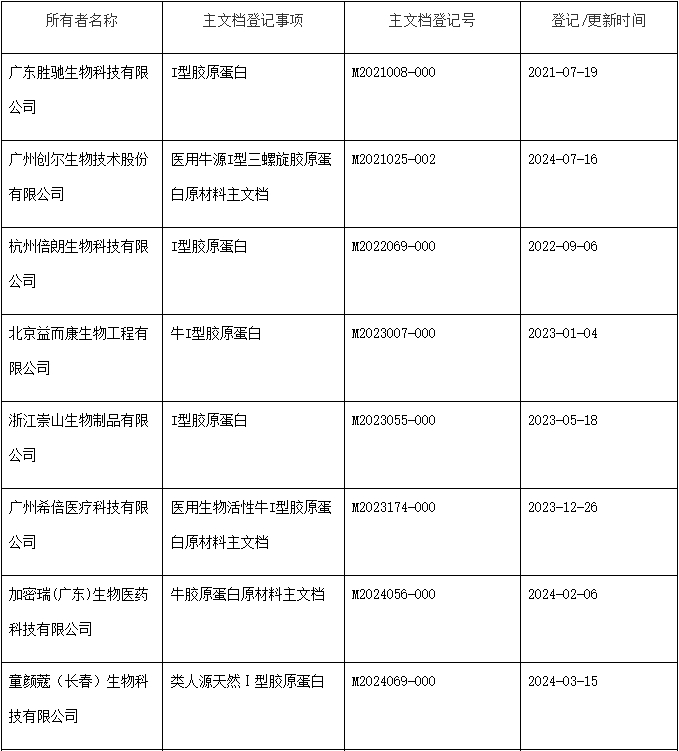
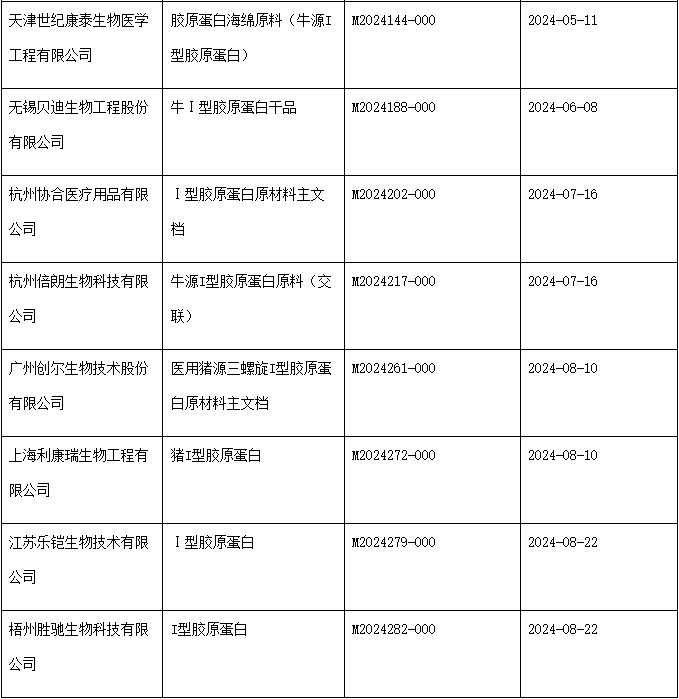
動物源膠原蛋白常用于醫美類產品,例如膠原貼敷料和整形用注射填充物。膠原貼敷料主要用于皮膚激光術后創面修復的輔助治療,整形用注射填充物主要用于糾正鼻唇溝紋和額部動力性皺紋。動物源膠原蛋白作為醫療器械產品原材料,可以進行主文檔登記,用于授權醫療器械注冊申請人在申報醫療器械注冊等事項時引用其作為注冊申報資料的一部分。
動物組織提取是膠原蛋白的主要來源之一。動物來源的膠原,比如豬源I型膠原蛋白、牛源I型膠原蛋白等,具有穩定的三螺旋結構,生物活性強,能夠起到較強的支撐作用。
但對于人體來說,動物源的膠原屬于異體膠原蛋白,可能攜帶具有傳染性的病原體,產生異體排斥反應。因此在注冊資料中應提交關于動物源性材料病原體滅活工藝的研究資料及降低免疫源性物質的工藝研究資料。供應商可將此部分資料進行主文檔登記。
醫療器械原材料(體外診斷試劑除外)的技術資料一般是指原材料組成成分描述、理化性能研究資料、生物學評價資料、毒理學風險分析資料等。
采用的膠原蛋白原料,應符合ASTM F2212—2009的要求。考慮到原料來自于動物, 會產生攜帶病毒的風險,應參照YY/T 0771.1、YY/T 0771.2、YY/T 0771.3進行管理。
生物學功能:動物源膠原蛋白主要生物學功能是為細胞提供支架和良好的微環境,可通過評價細胞-膠原蛋白相互作用來評價動物源膠原蛋白的生物學功能,比如細胞增殖、細胞分化、細胞粘附性、細胞的遷移或移行。
生物學評價:應按照GB/T 16886.1 的要求對動物源膠原蛋白進行相應必要的生物學評價。應在材料的化學表征、毒代動力學和有關毒性風險評價的科學數據基礎上進行毒理學評價。如有必要,還應該基于詳細測試并獲得數據后再進行毒理學評價。評價包括短期和長期的潛在影響,包括細胞毒性、刺激反應、致敏性、熱原、遺傳毒性、皮下植入、免疫原性、全身毒性和致癌性。
包裝、運輸和貯存:建議考慮相關醫療器械產品對原材料包裝、貯存、運輸的要求。
動物源膠原蛋白的性能指標如下(僅供參考):
1)理化特性
可研究外觀、可見異物、溶解性、水分灼燒殘渣、PH值、滲透壓摩爾濃度、動力粘度、熱穩定性、裝量及其差異、熔點。
2)鑒別
可研究肽圖、末端氨基酸序列、分子量、等電位。
3)純度
可通過電泳法或高效液相色譜法進行試驗。
4)雜質、污染物和添加劑
雜質檢測項目可能涉及到的項目有:雜蛋白分析、外源性DNA殘留量、殘余抗生素含量/活性、促炎性污染物(肽聚糖等)、重金屬及微量元素含量、添加劑等。
5)含量
可用總蛋白含量和純度計算。
6)結構表征
可通過特異性分析、一級結構的表征、紅外光譜、圓二色光譜、微量差熱分析、蛋白酶敏感性分析、脯氨酸羥基化分析、糖基化修飾分析進行研究。
7)安全性試驗
無菌、細菌內毒素、微生物限度等。

站點聲明
本網站所提供的信息僅供參考之用,并不代表本網贊同其觀點,也不代表本網對其真實性負責。圖片版權歸原作者所有,如有侵權請聯系我們,我們立刻刪除。如有關于作品內容、版權或其它問題請于作品發表后的30日內與本站聯系,本網將迅速給您回應并做相關處理。
鄭州思途醫療科技有限公司專注于醫療器械產品政策與法規規事務服務,提供產品注冊備案申報代理、臨床試驗、體系建立輔導、分類界定、申請創新辦理服務。

2019-12-01藥物臨床試驗機構(簡稱機構)開始實行備案管理。本文結合機構備案平臺構建思路,著重介紹了備案平臺的結構組成以及相關要求,梳理了機構備案過程中的常見問題,對機構

醫療器械臨床試驗與藥物臨床試驗在研究方法、統計方法、法規、程序等方面相近。藥物的致效機理基本相同,醫療器械的作用機理千差萬別,因此,醫療器械臨床試驗與藥物臨床試驗

90%的人忽略了女性CRA晉升到PM/LM/QM的難度,因為身體差異和社會歧視等因素,很多女性CRA晉升到manager的途徑其實是比較有限的,因此需要做好人生規劃和職業規劃才行。

根據《醫療器械監督管理條例》的規定,申請第二類、第三類醫療器械產品注冊,應當提交臨床評價資料,雖然《醫療器械監督管理條例修正案(草案送審稿)》(以下簡稱《修正案》)中提及

知情同意,指受試者被告知可影響其做出參加臨床試驗決定的各方面情況后,確認同意自愿參加臨床試驗的過程。改過程應當以書面的、簽署姓名和日期的知情同意書作為文件證明。對

醫療器械臨床試驗是初步的臨床人體安全、有效性的評價試驗。隨著科技的飛速發展,醫療器械的研發逐年增多,提高醫療器械臨床研究水平顯得更加重要。醫療器械的門類、功效非常

在臨床試驗中扮演著”大管家”這個角色的CRC,將越發舉足輕重。一個專業的CRC能協助研究者、申辦方有效高效地完成臨床試驗,作為一名合格的CRC,不僅要專業知識扎實,邏輯思維好

翻看以往各省藥監局的《醫療器械臨床試驗監督抽查工作通告》,統計了一下監查問題,發現存在臨床試驗數據存在不真實、不完整、無法溯源,臨床試驗質量低劣、相關記錄缺失等一系列問題

申辦方是自己成立監查員隊伍來做臨床研究,還是將臨床研究外包給CRO做,這個問題沒有標準答案。申辦方往往先是大量地將項目外包給CRO,一段時間后發現控制質量有問題,又收回來自己做。

在之前的文章中我們介紹了什么是藥械組合產品?以醫療器械為主的藥械組合產品如何申報注冊?本文將對藥械組合產品屬性界定情況進行介紹,匯總藥械組合注冊以來到2019年產品界定
行業資訊
知識分享
八年
醫療器械服務經驗
聯系思途,免費獲得專屬《落地解決方案》及報價
咨詢相關問題或咨詢報價,可以直接與我們聯系
思途CRO——醫療器械注冊臨床第三方平臺
